Campus
n°105 septembre-novembre 2011
Recherche | médecine
Attaque sur deux fronts contre le virus du sida
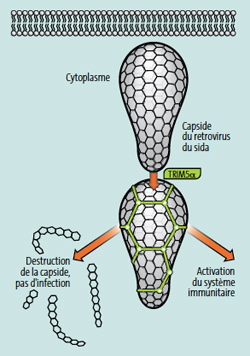
La protéine TRIM5alpha parvient à détruire le VIH quand celui-ci pénètre dans les cellules tout en mobilisant le système immunitaire pour se faire seconder. Une stratégie de défense naturelle qui manque d’efficacité chez l’humain mais qui représente une piste pour de futures thérapies
L’être humain n’est pas dénué d’armes naturelles face au virus du sida. Nos cellules disposent en effet d’un arsenal de protéines capables de l’attaquer à différents stades de l’infection. L’une de ces molécules s’appelle TRIM5alpha. Elle a pour mission de détruire la capside (l’enveloppe interne qui contient le matériel génétique de l’envahisseur) dès que celle-ci est relâchée dans le cytoplasme de la cellule hôte. Dans un article paru dans la revue Nature du 21 avril, l’équipe de Jeremy Luban, professeur au Département de microbiologie et médecine moléculaire (Faculté de médecine), vient de montrer que cette protéine possède une activité défensive additionnelle, celle de mobiliser le système immunitaire inné dès qu’elle détecte la présence de l’intrus, histoire de se faire seconder par une machinerie anti-infectieuse aguerrie. Au cas où.
Maladie incurable
Ces dispositifs sont très efficaces chez les singes de l’ancien monde, naturellement protégés contre le VIH et grâce auxquels l’action antirétrovirale de TRIM5alpha a d’ailleurs été découverte. Bien qu’existante également chez leur cousin, l’être humain, cette technique de défense est chez ce dernier, hélas, insuffisante, la réalité du sida étant là pour l’attester: plus de 25 millions de morts depuis 1981, date de l’identification de l’agent pathogène. Il n’en reste pas moins que chaque avancée dans la compréhension des mécanismes complexes de l’infection et la réplication du VIH dans les cellules humaines augmente les chances de développer un jour un remède ou un vaccin contre cette maladie aujourd’hui toujours incurable. D’où l’intérêt pour cette molécule qui a déjà fait l’objet de centaines de publications scientifiques.
Dans les premiers instants de l’infection, lorsque le virus se fixe sur la membrane de la cellule cible, il fusionne avec celle-ci et largue sa capside dans le cytoplasme. Cette structure en forme de poire est censée ensuite se désagréger afin de libérer les brins d’ARN viral qu’elle contient. C’est juste avant ce moment-là que TRIM5alpha intervient. La protéine enveloppe la capside encore intacte en tissant autour d’elle un filet à maille hexagonale. Elle démantibule ensuite sa proie de façon à ce que le matériel génétique soit inutilisable.
Le déroulement de ce scénario, à l’écriture duquel l’équipe de Jeremy Luban a contribué dès le début alors qu’il travaillait encore à l’Université Columbia à New York, était déjà connu. Dans son dernier article, le chercheur genevois et ses collègues complètent un peu plus l’histoire. Selon les auteurs, l’augmentation de la production de TRIM5alpha, consécutive à l’infection par le VIH, déclenche en parallèle une cascade de réactions qui aboutit à l’activation de certaines voies de signalisation du système immunitaire inné. Ce dernier comprend toutes les défenses de l’organisme qui n’impliquent pas la reconnaissance spécifique des agents infectieux (processus d’inflammation, mobilisation des globules blancs, alerte du système immunitaire adaptatif le cas échéant, etc.).
Jeremy Luban a également montré que TRIM5alpha joue le rôle d’un récepteur, sensible au «comportement» du rétrovirus du sida. Il semble que ce soit la structure même de la capside du VIH qui soit reconnue par la molécule défensive et que cette détection déclenche justement la réaction immunitaire. Toutes les expériences ont été menées in vitro, avec des cellules humaines et de singe.
Le fait que TRIM5alpha attaque le VIH sur deux flancs différents (destruction de la capside et mobilisation du système immunitaire inné) alors qu’il aurait pu se satisfaire d’un seul s’explique peut-être par le fait que, dans sa version simiesque en tout cas, son activité destructrice directe peut s’avérer insuffisante en cas de doses virales importantes. La réponse immunitaire innée pourrait alors protéger les cellules voisines, empêchant ainsi la propagation de l’agent infectieux dans l’organisme hôte.
La version humaine de TRIM5alpha, elle, est moins efficace peut-être parce qu’elle ne parvient pas à se lier convenablement avec la capside, ce qui expliquerait en partie qu’elle est incapable de prévenir l’infection. En revanche, il est possible que le fait que cette protéine active le système immunitaire (une action qui devrait encore être formellement observée in vivo) soit à l’origine de la très longue période d’incubation qui caractérise le VIH. Entre l’infection et la déclaration de la maladie, il se passe en effet en moyenne dix ans.
Tous ces éléments ouvrent la voie à des stratégies pour le développement de thérapies ou de vaccins contre le sida. Les perspectives sont néanmoins encore lointaines étant donné que ces mécanismes viennent à peine d’être découverts et que les chercheurs ne comprennent pas encore tout, tant s’en faut, et notamment pas les différences notables des défenses de l’homme et du singe face au VIH.
Anton Vos
