La microscopie à fluorescence s’attaque à la structure 3D des complexes protéiques
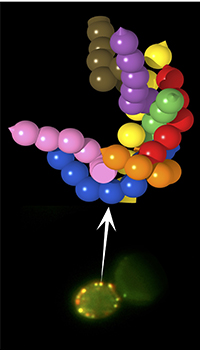
Nos cellules contiennent des structures de protéines responsables de l’exécution des fonctions cellulaires. L’une d’elles, l’exocyste, était encore un mystère pour les scientifiques jusqu’à ce jour. Bien que son rôle défini soit connu, sa structure et son organisation échappaient aux techniques de visualisation utilisées jusqu’alors. Des chercheurs de l’Université de Genève (UNIGE), en collaboration avec l’IRB Barcelone et le Centro Andaluz de Biologia del Desarollo à Séville, ont alors détourné une technique scientifique de son usage habituel afin de pouvoir reconstruire la structure en 3D de l’exocyste. Cette réussite, à lire dans la revue Cell, ouvre la voie à de nouveaux traitements qui permettraient de cibler les maladies dues à un dysfonctionnement de ces complexes protéiques.
L’exocyste est un complexe de huit protéines présent dans nos cellules qui permet la mise en contact des vésicules avec la membrane cellulaire et joue un rôle important dans la sécrétion d’insuline notamment. Lorsque l’exocyste dysfonctionne, elle provoque plusieurs maladies, dont le développement de métastases cancéreuses. C’est pourquoi les chercheurs ont cherché à comprendre sa structure et son fonctionnement. Les techniques traditionnelles utilisées dans ce cas sont la cristallographie ou la microscopie à électrons. Mais pour ce complexe particulier, grand et très flexible, aucune des deux techniques n’avait encore permis l’obtention d’un résultat probant. De plus, ces techniques obligent les chercheurs à travailler à l’extérieur de la cellule, en extrayant ces complexes protéiques dans des tubes permettant des analyses de structure in vitro. L’équipe du professeur Marko Kaksonen du Département de biochimie de la Faculté des sciences de l’UNIGE, en collaboration avec l’IRB Barcelone et le Centro Andaluz de Biologia del Desarollo à Séville, s’est alors intéressée à une technique connue, la microscopie à fluorescence qui n’a jamais été utilisée dans les reconstructions 3D de complexes protéiques.
«Pour réussir à modéliser l’exocyste, nous avons dans un premier temps modifié des cellules de levure afin de créer un point d’ancrage, c’est-à-dire une structure artificielle où l’on attache ce complexe protéique. Puis, grâce aux mesures prise par microscopie à fluorescence, nous avons pu marquer les différents éléments de la structure et la recréer de manière tridimensionnelle», explique Andrea Picco, chercheur à l’UNIGE. Ils ont ainsi pu recréer par trilatération la structure moléculaire de l’exocyste, tout en le faisant intégralement dans une cellule vivante permettant l’observation in vivo du rôle de ce complexe protéique, une première.
Cette réussite ouvre donc la voie à de nouveaux usages de la microscopie à fluorescence permettant ainsi d’obtenir des résultats sur de grandes structures de protéines, là où les techniques traditionnelles de reconstruction échouent. De plus, à présent que l’exocyste est modélisée en 3D et que sa structure et son organisation sont enfin comprises, les chercheurs vont pouvoir observer au plus près son mode de fonctionnement et les dysfonctionnements éventuels qui en découlent. «Nous savons maintenant comment fonctionne cette machinerie de huit protéines et ce pourquoi chaque protéine est importante. Cette connaissance nous aidera à mieux comprendre le processus de l’exocytose, son implication dans le cancer ou dans d’autres maladies et dès lors, d’envisager de nouveaux traitements», conclut Marko Kaksonen.
Contact: Marko Kaksonen, 022 379 69 97; Andrea Picco 022 379 69 94
27 janv. 2017