Régénération du muscle squelettique
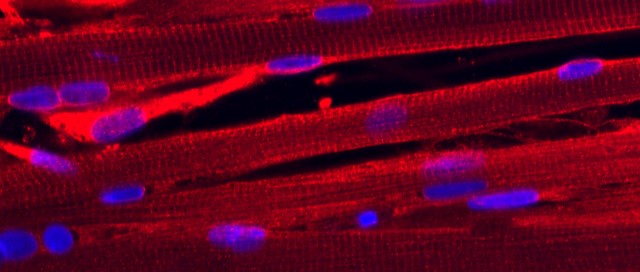
Nos muscles squelettiques sont capables de se réparer suite à des lésions, comme celles qui surviennent lors d’un exercice physique intense. La présence de courbatures après un effort est un des signes qui caractérise la mise en place des processus de régénération des cellules musculaires.
La réparation de ces grandes cellules plurinucléées à l’architecture interne très sophistiquée est possible grâce à la présence de cellules satellites, qui sont les cellules souches musculaires responsables de la régénération. Une altération des processus de réparation a de lourdes conséquences sur le maintien de la masse musculaire, et peut mener à diverses myopathies ou à une fonte musculaire chez les sujets âgés.
Nous étudions dans notre laboratoire le processus de régénération musculaire, en utilisant un modèle in vitro de culture de cellules musculaires à partir de cellules souches humaines.
