14 décembre 2021 - UNIGE
Le pied bot peut être causé par l’absence d’un interrupteur génétique
La mutation d’une courte séquence d’ADN contrôlant l’activation d’un gène impliqué dans le développement embryonnaire peut mener à des malformations.
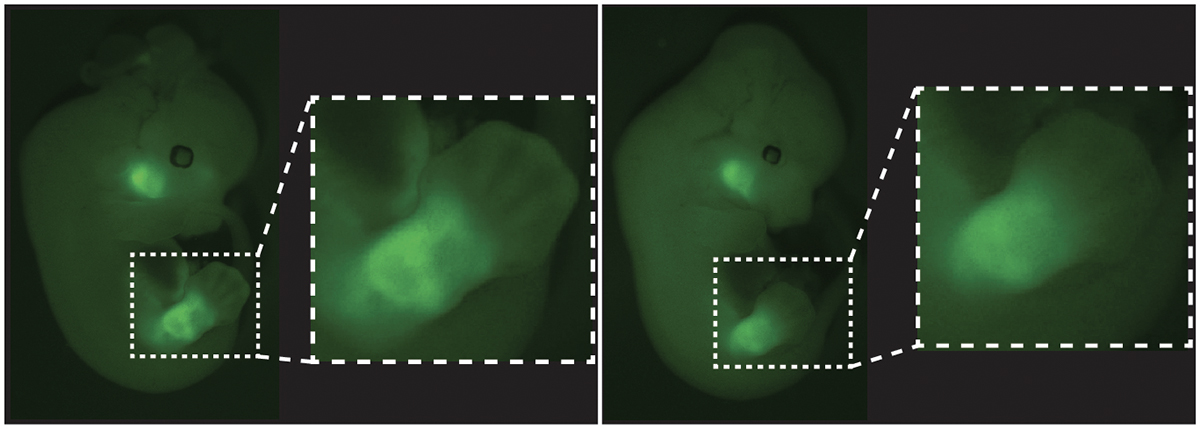
Visualisation par fluorescence de l’expression du gène Pitx1 dans des embryons de souris. À droite, l’absence de Pen, l’un des interrupteurs de Pitx1, se traduit par une perte de fluorescence dans les pattes antérieures. Image: G. Andrey/UNIGE
Le pied bot, une malformation courante des pieds, n’est pas forcément causé par le dysfonctionnement d’un gène impliqué dans le développement des membres inférieurs. Il peut aussi être dû à l’absence d’un de ses interrupteurs. C’est ce qu’a rapporté l’équipe menée par Guillaume Andrey, professeur au Département de médecine génétique et développement (Faculté de médecine), dans un article de la revue Nature Communications du 13 décembre. Lors du développement embryonnaire, des centaines de gènes doivent être activés ou réprimés avec précision afin de permettre la construction normale des organes. Ce contrôle d’activité est dirigé par de courtes séquences d’ADN qui, en liant certaines protéines dans le noyau cellulaire, agissent comme de véritables interrupteurs. «Lorsque l’interrupteur est allumé, cela lance la transcription d’un gène en ARN, qui à son tour sera traduit en une protéine, laquelle pourra alors exécuter une fonction précise, détaille Guillaume Andrey. Sans cela, les gènes seraient continuellement soit activés, soit désactivés et donc incapables d’agir de manière sélective, au bon endroit et au bon moment.»
-
Publié le
Comment nos organes savent-ils quand arrêter de grandir?
-
Publié le
Les échanges d'énergie renouvelable entre pairs a un impact positif pour l'individu, la communauté et le réseau

-
Publié le
La théorie quantique a besoin de nombres complexes

-
Publié le
L’absence d’un interrupteur génétique à l’origine de malformations

